Travaux Pratique :
SPECTRES
et MESSAGE DE LA LUMIERE
OBJECTIFS ::
- Distinguer
un spectre d’émission d’un spectre d’absorption.
- Reconnaître
et interpréter un spectre d’émission d’origine thermique
- Savoir
qu’un élément chimique ne peut absorber que les radiations qu’il est capable
d’émettre.
- Reconnaître
une entité chimique à partir d’un spectre.
En 1666, Isaac
Newton interprète la lumière du Soleil comme la superposition de radiations de
différentes couleurs. Un siècle et demi plus tard, les astronomes découvrent
que le spectre de la lumière solaire
est en fait plus complexe.
1.
ACTIVITE PREPARATOIRE :
ETUDE DE TEXTE : Dans l’Univers,
tout brille !
Etroite vision que celle de l’Homme
ayant comme seul attribut son œil nu ; pour appréhender le monde. Il ne peut
compter que sur la lumière des étoiles. Que le Soleil disparaisse, et Terre et
ciel sombreront dans le noir. C’est pourquoi, très tôt, on exploita
l’incandescence.
Chauffé convenablement, le
bois prend feu et la flamme qui en résulte crée un halo de lumière. Des siècles
plus tard, c’est le filament d’une lampe portée à incandescence qui éclaire la
nuit. Les étoiles émettent de la lumière visible et, à l’œil nu, on peut même
distinguer la lueur rouge de Bételgueuse (une étoile dont la température de surface
est de l’ordre de
PHOTOS CONSTELLATION
ORION
http://planet-terre.ens-lyon.fr/planetterre/objets/Images/rotation/orion1.jpg
1. Quelles
sont les sources de lumière citées dans le texte ?
2. A
partir du texte quelle hypothèse pouvez-vous émettre pour expliquer les couleurs
différentes des rayons lumineux émis par les étoiles ?
2. APPROCHE EXPERIMENTALE :
Les spectres seront visualisés grâce à
un spectroscope à réseau. Un réseau a le même effet dispersif sur la lumière
que le prisme vu en cours.
I-
Etude du spectre d’une lampe à incandescence.
Viser le filament de la lampe à incandescence à l’aide d’un spectroscope.
Observations :
Expérience : Observez le spectre quand la lumière est très faible. Quelles sont les couleurs qui ont disparu dans le spectre ?
Conclusion :
Fortement chauffé un corps solide, liquide ou gazeux émet un rayonnement
dont le spectre est ……………………. : c’est un SPECTRE D’EMISSION CONTINU.
La relation entre le spectre d’ continu et la température du corps ne dépend
pas du corps.
Quand la température du corps augmente le spectre se déplace vers les
radiations d’émission de couleurs ……………………..… et de longueurs d’ondes …………………
Application : Les étoiles ont des couleurs. Parmi elles, certaines sont plutôt rouges, d’autres plutôt bleutées. Quelles sont celles qui ont la température de surface la plus élevée ? la moins élevée ?
II- Etude de spectres de gaz excités
1. Lampes spectrales
Observer à l’aide de spectroscope à réseaux et comparer les lumières émises par les différentes lampes spectrales posées sur le bureau du professeur.
Décrire et représenter précisément les spectres de ces lampes en remplissant le tableau ci-dessous :
|
Nom de la lampe |
Couleur de la lumière émise |
Spectre d’émission de cette lampe |
|||
|
Lampe à vapeur de sodium |
|
|
|||
|
Lampe à vapeur de mercure |
|
|
2. Observation du spectre d’émission des lampes à tubes néons de la salle.
Observer à l’aide de spectroscope à réseau les lumières émises par les néons éclairant la salle de Travaux Pratiques.
1. Quel type de spectre
observez-vous ?
2.A partir de vos
observations, déduire le fonctionnement d’un tube néon.
Conclusion :
Un gaz chaud à basse pression émet des rayonnements dont le spectre
n’est pas ……………… : c’est un SPECTRES DE RAIES.
Ce sont des radiations monochromatiques caractéristiques de la nature
…………………… du gaz.
Le spectre …………………………………………. est une signature d’une espèce chimique.
III – Observations de
spectres d’absorption
1.
Absorption de la lumière par un filtre :
|
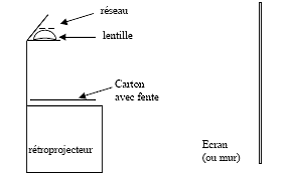
A l’aide du montage utilisant le
rétroprojecteur, on visualise le spectre de la lumière blanche. Ensuite, on place sur la fente du
carton, l’un après l’autre, plusieurs filtres colorés. On dessine les
spectres obtenus. |
|
|
Spectre de la lumière blanche |
|
|
Avec filtre bleu |
|
|
Avec filtre jaune |
|
|
Avec filtre rouge |
|
|
Avec filtre vert |
|
On en déduit que :
|
Le filtre bleu absorbe
………………………………………………………………. |
|
Le filtre jaune absorbe
………………………………………………………………. |
|
Le filtre rouge absorbe ………………………………………………………………. |
|
Le filtre vert absorbe
………………………………………………………………. |
2.
Absorption de la lumière par une
solution colorée
A l’aide du montage ci-dessous, on observe le spectre d’absorption de
différentes solutions colorées.
 Fente
Fente
Source
Solution Réseau Ecran
blanche colorée
Résultats :
|
Nom de la solution |
Couleur de la solution |
Spectre de la lumière |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Conclusion :
Le spectre de la lumière qui a traversé
une solution colorée présente des ……………..
………………… sur un fond ……………………. : c’est un SPECTRE DE BANDES
D’ABSORPTION.
Le spectre d’absorption d’une solution
de permanganate de potassium présente une bande noire dans les couleurs
……………… : la solution …………………….. donc ces couleurs.
Une solution colorée absorbe une partie
des couleurs de la lumière ………….. La couleur de la solution résulte de la somme
des couleurs …………………..
Le spectre d’absorption obtenu est caractéristique de ………………………………………….
Un gaz chaud à faible pression éclairé
en lumière blanche présente aussi un spectre de raies d’absorption
complémentaire au spectre de raies d’émission.
3. INITIATION A
L’ASTROPHYSIQUE :
I.
QUESTIONNEMENT :
1) Pourquoi ne peut-on pas effectuer une
étude in situ de la composition du Soleil en envoyant une sonde par
exemple ?
…………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………
2) Quelle est alors la seule solution
possible pour les astrophysiciens ?
…………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………
3) Expliquer quel type de spectre on
obtient en décomposant la lumière du Soleil et quel modèle simple permet
d’interpréter l’obtention de ce type de spectre :
…………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………
II.
DEMARCHE EXPERIMENTALE :
1)
A l’aide de ce premier lien, déterminer
les raies des atomes d’Hydrogène, de Carbone et d’Hélium.
http://www.ostralo.net/3_animations/swf/spectres_abs_em.swf
|
éléments |
Longueur d’onde des raies (nm) |
|||||||||
|
H |
|
|
|
|
|
|
|
|
|
|
|
He |
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
|
|
|
|
|
|
2)
A l’aide de ce second lien, déterminer
les longueurs d’ondes des raies d’absorption du spectre du soleil.
http://www.ostralo.net/3_animations/swf/spectres_soleil.swf
|
Longueur d’onde des raies (nm) |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3)
Identifier les éléments chimiques
correspondant à ces raies, ainsi que leur localisation (atmosphère terrestre ou
stellaire ?)
…………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………
FICHE TP :
MATERIEL : SPECTRES
et MESSAGE DE LA LUMIERE
Paillasse élève :
Spectroscopes portables.
Poste informatique + réseau.
Paillasse professeur :
- Lampes spectrales (Hg, Na).
- Poster des spectres d'émission.
- Générateur, rhéostat, lampe à incandescence, fils de connexion
- Montage d'absorption d’une solution colorée (prisme ou réseau, lentille, source, écran, cuve) avec des solutions de permanganate de potassium concentré et de sulfate de cuivre concentrée.
- Rétroprojecteur + réseau + fente en carton souple + filtre plastique rouge, jaune, verte, bleu. + écran