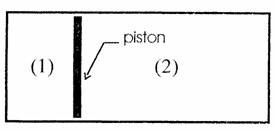
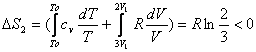Piston calorifugé (INA – ENSA) énoncé
Q1
V2 = 3 V1 initialement la température est To dans les 2 compartiments et chacun renferme le même nombre de mole, n = 1 mol
Lorsque le piston évolue vers son nouvel état d’équilibre la température du gaz à l’intérieur est égale à To. En effet les parois du piston sont parfaitement conductrices de la chaleur, et le thermostat extérieur est à la température To.
Tinitiale = Tf =T0
L’énergie interne est une grandeur extensive : l’énergie interne du système est égale à la somme de l’énergie interne du gaz du compartiment 1 et du compartiment 2. De plus l'énergie interne ne dépend que de la température car le gaz est parfait :
![]()
Q2
Réponse partielle pour voir la correction vidéo clique ici.
L'ensemble
![]()
est isolé, donc :
![]()
![]()
Q3
L’entropie du système S augmente car la transformation est
irréversible.
![]()
La transformation est irréversible, donc :
![]()
donc
![]()
Calcul de l’entropie créé. Réponse partielle pour voir la
correction vidéo clique ici.
![]()
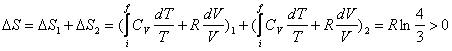
Q4
Réponse partielle pour voir la correction vidéo clique ici.
L’entropie du système 2 diminue ; en effet :
![]()
avec n = 1 mol