|
|
Chapitre 18 : composés organiques oxygénés |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Cours écrit 1) rappel sur le nom des 5 premiers alcanes à
chaine linéaire 2) Comment reconnaitre un alcool? 1) différence entre aldéhyde et cétone 2) règles de nomenclature des aldéhydes et cétones 1) définition d'un acide carboxylique 2) nomenclature des acides carboxyliques 3) propriétés chimiques des acides carboxyliques Cours vidéointroduction:
quelques composés oxygénés I) les alcools 1) rappel sur le nom des 5
premiers alcanes 2) comment reconnaitre un
alcool? II) aldéhydes et cétones 1) différence entre
aldéhydes et cétones 2) règles de nomenclatures des aldéhydes et cétones III) les acides
carboxyliques 1) définition d'un acide carboxyique 2)
nomenclature des acides carboxyliques 3) propriétés chimiques des acides |
Introduction:
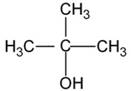
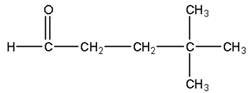
animation: représentation spatiale des molécules Voici quelques composés organiques oxygénés:
Un composé organique oxygéné provient d'une espèce vivante. Il contient une chaine carbonée et un ou plusieurs atomes d'oxygène. On différencie un composé organique oxygéné d'un autre à l'aide de son groupe caractéristique. I)
Les alcools
1)
rappel sur le nom des 5 premiers alcanes à chaine linéaire
Les alcanes à chaine linéaire sont constitués à partir de carbone tétragonal (lié à 4 autres atomes) et d'atomes d'hydrogène. Leur formule brute générale est CnH2n+2. Leur nom doit être connu car on va utiliser le préfixe pour nommer les composés oxygénés. maman est partie bébé pleure méthane éthane propane butane pentane
2)
Comment reconnaitre un alcool?
Un
alcool est caractérisé par un groupement hydroxyle -OH, lié à un carbone
tétragonal (carbone lié à 4 autres atomes). Cet atome est appelé carbone
fonctionnel. Le
groupe hydroxyle est appelé le groupe caractéristique ou groupe
fonctionnel des alcools. La
formule brute générale des alcools saturés (liaison covalente simple entre
les atomes de carbone et d'hydrogène) est CnH2n+2O Remarque:
lorsque
la chaîne carbonée contient des insaturations cette formule n'est plus
valable donc il ne s'agit plus d'alcool. Exercice:
le
cyclohexanol est t-il un alcool? formule topologique
formule brute C6H12O Réponse: non car sa formule brute n'est pas de la forme CnH2n+2O 3)
Les 3 classes d'alcool
Un
alcool est primaire si le carbone fonctionnel est lié à 1, ou 0 atome de
carbone Formule
générale R-CH2-OH ou (CH2OH) (avec
R, chaîne carbonée) Un
alcool est secondaire si le carbone
fonctionnel est lié à 2 atomes de carbone Formule
générale (R et R' chaîne carbonées)
Un
alcool est tertiaire si le carbone fonctionnel est lie à 3 atomes de carbone. Formule
générale (R, R'et R'' chaîne carbonées) :
Exemple:
II)
aldéhyde et cétone
1)
différence entre aldéhyde et cétone
2 exemples...
Les aldéhydes et les cétones sont des composés oxygénés
qui contiennent le groupe carbonyle Ils sont appelés composés
carbonylés. Le carbone fonctionnel est celui du groupe carbonyle. Il est
trigonal (lié à 3 autres atomes)
Les autres carbones sont tétragonaux (liés à 4 autres atomes). La formule
brute générale des composés carbonylés est CnH2nO. Un composé carbonylé dont le carbone fonctionnel est lié à au moins un atome d'hydrogène est un aldéhyde. Sa formule générale est:
R: hydrogène ou chaîne carbonée Exemple: le méthanal (appelé également formol)
L'éthanal
Un composé carbonylé dont le carbone fonctionnel est lié à 2 atomes de carbone est une cétone. Sa formule générale est:
R et R' : chaîne carbonée Exemple: le pentan-2-one
2)
règles de nomenclature des aldéhydes et cétones
Pour établir le nom des composés carbonylés que sont les aldéhydes et cétones 1. on recherche la chaîne la plus longue comportant l'atome de carbone fonctionnel 2. on numérote les atomes de carbone en minimisant l'indice du carbone fonctionnel 3. on repère les ramifications alkyle sur la chaîne principale, on écrit le numéro du carbone portant la ramification, puis un tiret et enfin le nom de la ramification avant le nom de la chaîne principale. 4. on remplace le e de l'alcane correspondant par la terminaison al pour les aldéhydes et one pour les cétones. Exemples:
III)
les acides carboxyliques
1)
définition d'un acide carboxylique
Quelques
exemples:
Un
acide carboxylique présente le groupe caractéristique carboxyle:
La
formule générale des acides carboxyliques est: R-CO2H
avec R:
chaîne carbonée ou atome d'hydrogène Le
carbone fonctionnel est trigonal (lié à 3 autres atomes). La
formule brute générale d'un acide carboxylique est: CnH2nO2 2) nomenclature des acides
carboxyliques
Pour établir le nom des acides carboxyliques 1. on recherche la chaîne la plus longue comportant l'atome de carbone fonctionnel 2. on numérote les atomes de carbone en minimisant l'indice du carbone fonctionnel 3. on repère les ramifications alkyle sur la chaîne principale, on écrit le numéro du carbone portant la ramification, puis un tiret et enfin le nom de la ramification avant le nom de la chaîne principale. 4. Le nom du composé est précédé du mot acide. On remplace ensuite le "e" du nom de l'alcane correspondant par la terminaison "oïque". Exemple:
3)
propriétés chimiques des acides carboxyliques
Les acides carboxyliques sont-ils solubles dans l'eau?
L'acide éthanoïque (10 % environ du vinaigre) est très
soluble dans l'eau. Cette solubilité est due à l'établissement de liaison
hydrogène entre les molécules d'eau (solvant polaire) et le groupe carboxyle.
Le groupe carboxyle est hydrophile. Par
contre la chaîne carbonée de l'acide carboxylique est apolaire. Par
conséquent elle est hydrophobe. L'acide pentanoïque (CH3-CH2-CH2-CH2-COOH) est t-il plus soluble que l'acide éthanoïque? Non car sa chaine carbonée hydrophobe est plus longue que la chaine carbonée de l'acide éthanoïque. La solubilité des
acides carboxyliques dans l'eau est due au groupe carboxyle qui est
hydrophile. Ce groupe établit des liaisons hydrogène avec les molécules d'eau La solubilité des
acides carboxyliques diminue lorsque la longueur de la chaine carbonée
augmente. Pourquoi qualifier d'acide les acides carboxyliques? L'acide éthanoïque réagit avec l'eau suivant l'équation chimique: CH3CO2H(aq) + H2O -> CH3CO2-(aq) + H3O+(aq) Il y a production d'ion oxonium (ou hydronium) H3O+. Par conséquent le milieu devient acide ( pH < 7). La molécule d'acide s'ionise. Le caractère acide d'une solution aqueuse d'acide carboxylique est dû à son ionisation au contact des molécules d'eau. Il y a production d'ions oxonium (ou hydronium) H3O+. Le pH de la solution diminue. Equation chimique correspondante: R-CO2H(aq) + H2O -> R-CO2-(aq) + H3O+(aq) Exercice: écrire l'équation chimique correspondant à la réaction chimique entre l'acide propanoïque et l'eau: CH3-CH2-CO2H(aq) + H2O -> CH3-CH2-CO2-(aq) + H3O+(aq) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|