chapitre 5 : constante d’acidité d’un couple acide base
pH d’un un mélange corrigé
Dans cet exercice, on se propose de calculer la
valeur du pH d’un mélange de deux solutions de pH connus.
Données : pKa1 (HNO2
/ NO2–) = 3,3
pKa2
(HCOOH / HCOO–) = 3,8
pKe
= 14,0
I – ÉTUDE DE DEUX
SOLUTIONS
Le pH d’une solution aqueuse d’acide
nitreux HNO2(aq), de concentration en soluté apporté
C1 = 0,20 mol.L-1 a pour valeur pH1 =
2,0 ; celui d’une solution aqueuse de méthanoate de sodium (HCOO–(aq)
+ Na+(aq)) de concentration en soluté apporté C2
= 0,40 mol.L-1 a pour valeur pH2 = 8,7.
1. a) Écrire
l’équation de la réaction entre l’acide nitreux et l’eau. Donner l’expression
de sa constante d’équilibre.
b) Écrire
l’équation de la réaction entre l’ion méthanoate et l’eau. Donner l’expression
de sa constante d’équilibre.
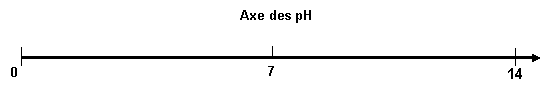
2. a)
Sur l’axe des pH, donné en annexe à rendre avec la copie, placer les
domaines de prédominance des deux couples acide/base mis en jeu.
b) Préciser
l’espèce prédominante dans chacune des deux solutions précédentes.
II
– ÉTUDE D’UN MÉLANGE DE CES SOLUTIONS
1. On
mélange un même volume v = 200 mL de chacune des deux solutions précédentes. La
quantité de matière d’acide nitreux introduite dans le mélange est n1
= 4,0 ´
10-2 mol et celle de méthanoate de sodium est n2 = 8,0 ´ 10-2 mol.
a)
Écrire l’équation de la réaction qui se produit
lors du mélange entre l’acide nitreux et l’ion méthanoate.
b)
Exprimer, puis calculer, le quotient de réaction Qr,i
associé à cette équation, dans l’état initial du système chimique.
c)
Exprimer le quotient de réaction dans l’état
d’équilibre Qr,éq en fonction des constantes d’acidité des couples
puis le calculer.
2. a) Compléter le tableau
d’avancement, donné en annexe à rendre avec la copie.
b) La valeur de l’avancement final, dans cet état
d’équilibre est : xéq = 3,3 ´
10-2 mol.
Calculer
les concentrations des différentes espèces chimiques présentes à l’équilibre.
c) En déduire la valeur de Qr, éq et la
comparer à la valeur obtenue à la question 1. c).
3. À
l’aide de l’un des couples intervenant dans le mélange, vérifier que la valeur
du pH
du mélange est proche de la valeur pH3 = 4.
EXERCICE
III
ANNEXE A RENDRE AVEC LA COPIE
Tableau
d'avancement de la transformation
entre l'acide nitreux et le méthanoate de sodium
|
Équation |
…………. +
…………. = ………….
+ …………. |
||||
|
État du système chimique |
Avancement (mol) |
Quantités de matière (mol) |
|||
|
n(HNO2(aq)) |
n(HCOO–(aq)) |
…………. |
…………. |
||
|
État initial |
x = 0 |
n1 |
n2 |
|
|
|
État intermédiaire |
x |
|
|
|
|
|
État d’équilibre |
x = xéq |
|
|
|
|