Chapitre 6 : réaction acido-basique, titrage
Réactions acido-basiques (Afrique 2003) corrigé
1. Identification d'un indicateur coloré.
On dispose d'un flacon
d'indicateur coloré avec comme seule indication sa concentration molaire :
C0 = 2,9.10-4 mol.L-1 .On mesure son pH: 4,18.
On en déduit la concentration molaire en ions oxonium [H3O+]
= 6,6.10-5 mol.L-1.Le couple acide/base présent dans cet
indicateur coloré sera noté HInd/Ind–. La solution d'indicateur coloré
a été préparée à partir de la forme acide de l'indicateur : HInd. L'équation de
la réaction entre HInd et l'eau est : HInd + H2O
= Ind– + H3O+
1.1 En considérant un volume V=100 mL de solution d'indicateur, déterminer le taux d'avancement final de la réaction de l'acide HInd avec l'eau.Cet acide est-il totalement dissocié dans l'eau ? Justifier votre réponse.
1.2 Donner l'expression littérale de la constante d'acidité KA de la réaction de l'acide HInd sur l'eau.
1.3 Les concentrations à l'équilibre permettent de calculer la constante d'acidité de la réaction : KA=1,9.10-5., calculer le pKA du couple Hind/Ind– et identifier l'indicateur à l'aide des données du tableau suivant :
|
Indicateur |
Couleur acide |
Zone de virage |
Couleur |
pKA |
|
Hélianthine |
Jaune orangé |
3,1 – 4,4 |
Rouge |
3,7 |
|
Vert de Bromocrésol |
jaune |
3,8 – 5,4 |
Bleu |
4,7 |
|
Bleu de Bromothymol |
jaune |
6,0 – 7,6 |
Bleu |
7,0 |
|
Phénolphtaléine |
incolore |
8,2 – 10,0 |
Fuschia |
9,4 |
2. Dosage d'une
solution d'acide chlorhydrique concentrée.
Dans le laboratoire d'un lycée, on dispose d'un flacon d'une solution d'acide chlorhydrique concentrée où est notée sur l'étiquette l'indication suivante : 33% minimum en masse d'acide chlorhydrique. On appellera cette solution S0. On veut connaître la concentration molaire c0 de cette solution.
Première étape :On dilue 1000 fois la solution S0 . On obtient alors une solution S1 de concentration C1.
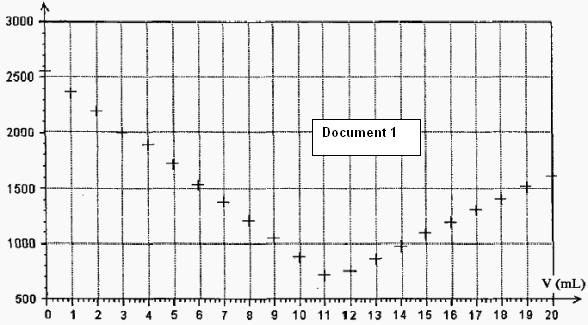
Deuxième étape : On prélève précisément un volume V1=100,0 mL de solution S1. On dose par conductimétrie la solution S1 par une solution titrante d'hydroxyde de sodium de concentration CB= 1,00.10-1 mol.L-1. La représentation graphique de la conductance de la solution en fonction du volume V de solution titrante versé est donnée dans l'annexe 2, document n°1.
2.1 On ajoute la solution d'hydroxyde de sodium pour doser la solution S1. Écrire l'équation de la réaction acido-basique.
2.2 Déterminer graphiquement, sur le document n°1 de l'annexe 2, le volume versé VE à l'équivalence.
2.4 En déduire la concentration molaire C0 de la
solution d'acide chlorhydrique concentrée S0.
2.5 Calculer la masse m0 d'acide chlorhydrique (H3O+
aq + Cl- aq ) dissous dans un litre de solution.
On donne la masse molaire de l'acide chlorhydrique M=
2.6 La solution S0 a une masse volumique ρ0 =
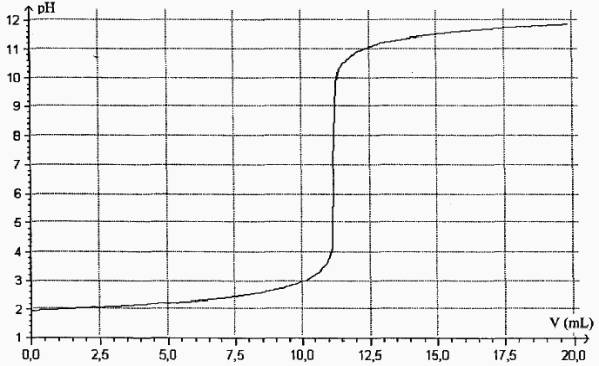
2.7 Une simulation du dosage par suivi pH-métrique de la solution S1 est donnée dans l'annexe 2, document n°2. Sur le document n°2, indiquer la la couleur de la solution ainsi que l’espèce chimique prédominante de l’indicateur coloré.
2.8 Dans la liste donnée à la question 1.3, y-a-t-il un indicateur coloré mieux adapté pour repérer l'équivalence du dosage ? Justifiez votre réponse.
Attention : L’annexe 2 est à rendre avec votre copie.
Annexe 2 : À rendre
avec la copie
Document n°1 : Dosage de la solution diluée d'acide
chlorhydrique S1 par conductimétrie
Document n°2 : Simulation du dosage de la solution diluée
d'aide chlorhydrique S1 par pHmétrie