A propos de l’acide
formique (USA Bac 2004) énoncé
Q1
a) Calcul de la masse m d’acide formique.
Co = 0,01 mol.L-1 ; Vo = 100 mL = 0,1 L; M(HCOOH) = 2.M(H) + M(C) + 2.M(O) = 2 + 12 +
2x16 = 46 g.mol-1

Pour préparer la solution, il faut utiliser
0,046 g d’acide formique.
b) Réaction acido-basique entre l’acide
formique et l’eau :
HCOOH aq +
H2O(l) = HCOO-aq
+ H3O+aq
Pour les étourdi(e)s : n’oubliez pas
d’indiquer dans quel état se trouvent les espèces chimiques (aqueuse pour les
ions).
Q2
a) Tableau d’avancement :
|
Equation de
réaction |
HCOOH + H2O = HCOO- +
H3O+ |
||||||
|
Etat du système |
Avancement en mol |
Quantité
de matière en mol
|
|||||
|
Etat initial |
O |
Co.Vo |
excès |
0 |
0 |
|
|
|
Etat final (si la réaction était totale) |
xmax |
CoVo-xmax= 0 |
excès |
xmax |
xmax |
|
|
|
Etat d’équilibre (transformation non totale) |
xeq |
CoVo - xeq |
excès |
xeq |
xeq |
|
|
b) Réponse partielle, pour voir la correction
vidéo clique
ici.
Expression de t en fonction de [H3O+]eq et de Co :
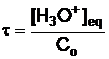
c) Réponse partielle, pour voir la correction
vidéo clique
ici.
Expression du quotient de réaction à
l’équilibre Qreq:
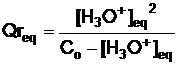
2 remarques : l’eau n’intervient pas dans
l’équation bilan, car il s’agit du solvant. D’après le tableau d’avancement
précédent, la concentration en ion méthanoate (ou
formiate) est identique à celle de l’ion oxonium.
Q3
a) Réponse partielle, pour voir la correction
vidéo clique ici.
Conductivité s de la solution :
s = [H3O+]eq
. ( l(H3O+) + l(HCOO-) )
b) Réponse partielle, pour voir la correction
vidéo clique
ici.
|
Solution |
So |
S1 |
|
Ci(mol.L-1) |
0,010 |
0,10 |
|
s(S.m-1) |
0,050 |
0,17 |
|
[H3O+]eq (mol.m-3) |
1,24 |
4,2 |
|
[H3O+]eq (mol.L-1) |
1,24 x 10-3 |
4,2 x 10-3 |
|
t(%) |
12,4 |
4,2 |
|
Qreq |
1,76 x 10-4 |
1,8 x 10-4 |
c) La valeur du quotient de réaction à l’équilibre
est peu différente de celle de la constante d’acidité :
Qreq = 1,76 x10-4 » KA = 1,8 x 10-4
Q4
a) Plus la solution est diluée plus le taux
d’avancement augmente :
C( So )
< C(S1) Þ t (So) > t (S1)
|
Solution |
So |
S1 |
|
Ci(mol.L-1) |
0,010 |
0,10 |
|
t (%) |
12,4 |
4,2 |
b) La concentration de la solution n’a pas
d’influence sur le quotient de réaction :
Qr,eq (So) » Qr,eq (S1)
|
Solution |
So |
S1 |
|
Ci(mol.L-1) |
0,010 |
0,10 |
|
Qreq |
1,76 x 10-4 |
1,8 x 10-4 |