Véto 98 énoncé
Q1
Macroscopiquement
le gaz parfait est régit par l’équation d’état :
pV = nRT ;
Microscopiquement :
Pour un
gaz parfait : son énergie d’interaction par molécule est négligeable
devant l’énergie cinétique des molécules (kT) : l’énergie interne d’un gaz
parfait ne dépend que de sa température.
Q2

Compartiment B : V = 1000 L ; corps de pompe
A, volume max : Vo = 10 L ;Opération de vidage isotherme et quasi
statique
Début d’opération : air et extérieur à To = 298
K ;po = 105 Pa
Pour un aller retour le piston prélève une certaine
quantité de matière ‘n’ du compartiment B,
puis la rejette dans l’atmosphère. Cette quantité de matière représente
un volume Vo =
![]()
Le nombre de mole initial ‘ni’ contenu dans le
compartiment B (po, V, To) est :
![]()
Après un aller retour il ne reste que la quantité de
matière nf dans le compartiment B :
![]()
Par conséquent la pression finale p1 dans le
compartiment B est :
![]()
Q3
Remarque :
A l’aller le gaz contenu dans le compartiment A est rejeté vers l’extérieur. Le
gaz contenu dans le piston ne subit aucune modification et ne reçoit ni fournit
de travail
Le travail
reçu par le gaz n’existe que pendant le retour du piston ; le gaz se
détend du volume V au volume V+Vo à la température To. La transformation étant
quasi statique en chaque instant P(extérieure) = P(intérieure = nRT/V)
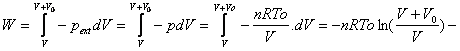
or
![]()
![]()
Remarque :
ce travail est négatif car le gaz en se détendant fournit du travail au piston.
Q4
travail du moteur est
![]() .
.
a)
Réponse partielle pour voir la correction
vidéo clique ici.
DU = 0
, car la température est inchangée.
Comme
l’entropie d’un gaz parfait est
![]()
et comme l’entropie de l’air expulsé dans
l’aller ne varie pas, la variation d’entropie est celle de l’air qui reste
enfermé, soit
![]() .
.
b)
Réponse partielle pour voir la correction
vidéo clique ici.
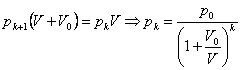
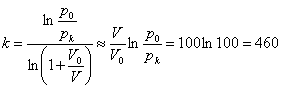 .
.