Chapitre 2 : suivi temporel d’une
réaction chimique corrigé
Teneur en CO2 d’un vin (Liban
2006 3 points)
Le vin est obtenu par fermentation
du jus de raisin.
Lors de la fermentation alcoolique,
le glucose présent dans le raisin est dégradé en
éthanol et en dioxyde de carbone CO2. Lorsque la vinification
est terminée, on décèle généralement dans le
vinla présence de CO2 à raison de 200 à 700 mg
par litre.
Pour déterminer la
concentration en CO2 d’un vin, les laboratoires
d’œnologie analysent, par spectrophotométrie, les
échantillons que leur fournissent les viticulteurs.
A l’aide d’un
spectrophotomètre, l’absorbance de cet échantillon est
mesurée pour une gamme de longueurs d’onde données
(situées de part et d’autre du maximum d’absorption dû
à la présencede CO2). Ces mesures sont ensuite
reportées sur un graphe constituant le spectre d’absorption de
l’échantillon pour la gamme de longueurs d’onde choisie.
Dans tout cet exercice on considèrera
que dans la gamme de longueurs d’onde choisies, seul le CO2
absorbe.
Un élève cherche
à déterminer la concentration en CO2 d’un
échantillon de vin. Il dispose pour cela de quatre autres
échantillons de vin de concentration en CO2 connues :
Échantillon
n°1 C1
= 4,5 mmol.L-1
Échantillon
n°2 C2
= 10,4 mmol.L-1
Échantillon
n°3 C3
= 24,3 mmol.L-1
Échantillon
n°4 C4
= 29,5 mmol.L-1
Échantillon
n°5 C5
à déterminer
Il réalise le spectre
d’absorption de chacun de ces échantillons et obtient le graphe de
l’absorbance en fonction de l’inverse de la longueur d’onde
(le nombre d’onde 1/l)
donné ci-dessous :
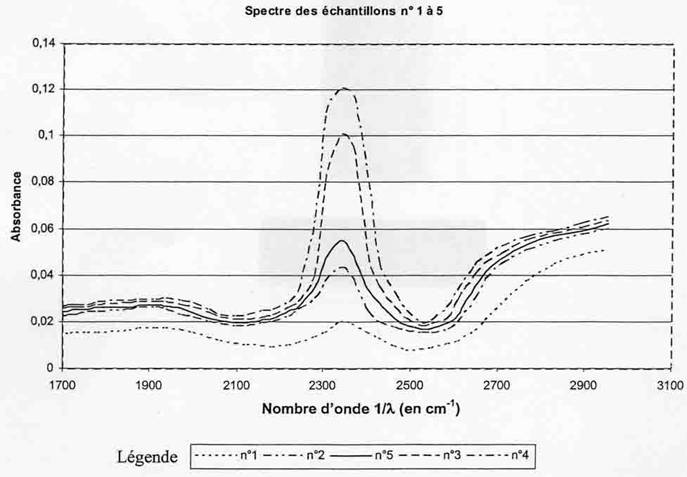
1. On se place, pour chaque échantillon, au
maximum d’absorption dû au CO2.
a) Déterminer graphiquement la
valeur de l’absorbance pour le maximum d’absorption de chaque échantillon.
b) Tracer la courbe
d’étalonnage A = f (C) représentant l’absorbance de
la solution en fonction
de la concentration en CO2 de l’échantillon.
c) Quelle est l’allure de la
courbe tracée à la question 1.b) ? Sans aucun calcul que
peut-on en déduire ?
2. La loi de Beer-Lambert.
a)
Exprimer l’absorbance A en fonction
de la largeur de la cuve L, du coefficient d’extinction molaire ![]() et de la concentration C de la solution.
et de la concentration C de la solution.
b)
La courbe obtenue à la question 1.b) vous semble-t-elle en accord
avec cette loi ?
c) Utiliser cette courbe pour
déterminer la valeur du coefficient e, en unités SI, sachant que L = 3,5.10-
3. a) A l’aide de la courbe, A =
f(C), déterminer la concentration en CO2 de
l’échantillon inconnu n°5.
Expliciter
clairement la démarche suivie.
b) Le vin
contenu dans cet échantillon entre-t-il dans la catégorie des vins
cités dans le texte
(en ce qui concerne sa teneur en CO2) ?
Données : M(C) =