|
Cours :
 
Fiches méthodes
Puissances de
10, notation scientifique
 
Unités légales
du système international / conversion
 
Méthode de
résolution d’exercices
 
Résoudre une
équation à une inconnue
 
 
Programme officiel
|
Notions et contenus
|
Capacités exigibles
Activités expérimentales support de la formation
|
|
A) Description et caractérisation de la matière à l’échelle
macroscopique
|
|
Corps purs et mélanges au quotidien.
Espèce chimique, corps pur, mélanges d’espèces chimiques, mélanges
homogènes et hétérogènes.
|
Citer des exemples courants de corps purs et de mélanges homogènes
et hétérogènes.
|
|
Identification d’espèces chimiques dans un échantillon de matière
par des mesures physiques ou des tests chimiques.
|
Citer la valeur de la masse volumique de l’eau liquide et la
comparer à celles d’autres corps purs et mélanges.
Distinguer un mélange d’un corps pur à partir de données
expérimentales.
Mesurer une température de changement d’état, déterminer la masse
volumique d’un échantillon, réaliser une chromatographie sur couche mince,
mettre en oeuvre des tests chimiques, pour identifier une espèce chimique
et, le cas échéant, qualifier l’échantillon de mélange.
|
|
Composition massique d’un mélange.
Composition volumique de l’air.
|
Citer la composition approchée de l’air et l’ordre de grandeur de
la valeur de sa masse volumique.
Établir la composition d’un échantillon à partir de données
expérimentales.
Mesurer des volumes et des masses pour estimer la composition de
mélanges.
Capacité mathématique : utiliser les pourcentages et les
fractions.
|
|
1. densité
de l’heptane (ds)
2. densité de l’acétone et du mercure
3. miscibilité de H2O, menthone, éthanol
4. extraction du cinéol (ds) WORD PDF
5. présence de caféine dans une pommade ?
WORD PDF
6. ds 4/10/2019 : chromatographie ;
densité ; masse volumique ; changements d’état
WORD PDF
|
1. Conversions et mesures de volume
et de masse

2. Comment
mesurer la masse volumique d’un solide ?
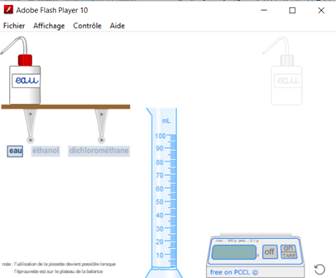
3. Changement d’état de l’eau
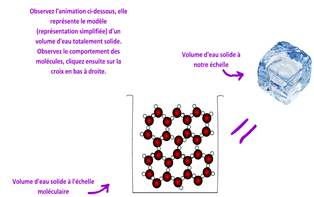
4. CEA : les 3 états de la
matière

5. Changement d’état d’un
corps pur, l’eau
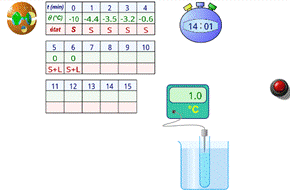
|
1. mise en évidence de la présence d’eau avec
le sulfate de cuivre anhydre
2. mise en évidence de la
présence de CO2
3. mise en évidence de la
présence de H2
4.
principe de la chromatographie
5. écriture scientifique d’un
résultat
|






