|
|
|
Le
cortège électronique de l’atome définit ses propriétés chimiques.
Configuration
électronique (1s, 2s, 2p, 3s, 3p) d’un atome à l’état fondamental et
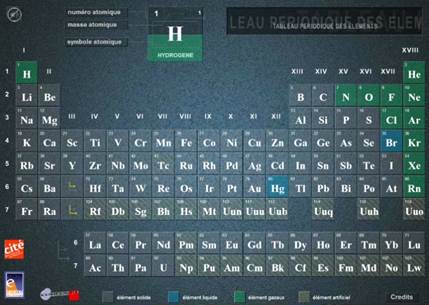
position dans le tableau périodique (blocs s et p).
Électrons
de valence.
Familles chimiques.
|
|
|
Déterminer
la position de l’élément dans le tableau périodique à partir de la donnée
de la configuration électronique de l’atome à l’état fondamental.
Déterminer
les électrons de valence d’un atome (Z ⩽ 18)
à partir de sa configuration électronique à l’état fondamental ou de sa
position dans le tableau périodique.
Associer la notion de famille chimique à l’existence
de propriétés communes et identifier la famille des gaz nobles.
|
|
|
Vers
des entités plus stables chimiquement.
Stabilité
chimique des gaz nobles et configurations électroniques associées.
Ions
monoatomiques.
|
|
|
Molécules.
Modèle
de Lewis de la liaison de valence, schéma de Lewis, doublets liants et
non-liants.
Approche
de l’énergie de liaison.
|
|
|
|
|
|
|
Établir le
lien entre stabilité chimique et configuration électronique de valence d’un
gaz noble.
Déterminer
la charge électrique d’ions monoatomiques courants à partir du tableau
périodique.
Nommer les
ions : H+, Na+, K+, Ca2+, Mg2+, Cl-, F- ; écrire leur formule à partir de
leur nom.
Décrire
et exploiter le schéma de Lewis d’une molécule pour justifier la
stabilisation de cette entité, en référence aux gaz nobles, par rapport aux
atomes isolés (Z ⩽ 18).
Associer qualitativement l’énergie d’une liaison entre
deux atomes à l’énergie nécessaire pour rompre cette liaison.
|